Eine lebende Zelle hat kein entspanntes Dasein: Ständig muss sie ihre Gestalt anpassen. Wenn sie sich teilt, muss sie ihre gesamte Form massiv umbauen. Wenn sie Stoffe aufnimmt, muss sie ihre äußere Membranhülle stark verformen. Und wenn sie auf Wanderschaft geht, muss sie zunächst einmal entscheiden, wo vorne und wo hinten ist, dann ihre eingebauten molekularen Motoren anwerfen und so die Fortbewegung in Gang setzen.
Zellen sind lebende Gebilde mit vielen dynamischen Funktionen. Die Fähigkeit einer Zelle, ihre Form zu ändern, ist dabei entscheidend. Bei der Zellteilung spielen diese Prozesse eine wichtige Rolle, bei Wundheilung oder Embryonalentwicklung, aber auch, wenn Krebszellen sich im Körper ausbreiten.
Wie sich eine Zelle spontan mit Hilfe einiger weniger Komponenten verformt, untersuchten Forscher um den Biophysiker Andreas Bausch, Inhaber des Lehrstuhls für Zellbiophysik an der TU München und Mitglied des Exzellenzclusters Nanosystems Initiative Munich, nun mit einem einfachen Zellmodell genauer. Der Nachbau soll helfen, die Funktionen des komplexen Zellsystems besser zu verstehen.
Modellzelle zur Untersuchung der Zellmechanik
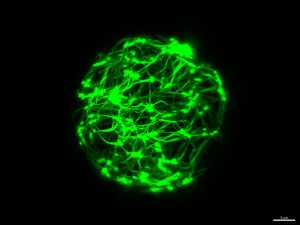
Die Hülle der Modellzelle besteht aus einer zweischichtigen Lipidmembran, ganz analog zu natürlichen Zellmembranen. In dieses Vesikel füllten die Forscher gezielt Biomoleküle, die in Körperzellen wichtige Funktionen haben. Bei ihren Versuchen zur Verformung der Zellen verwendeten sie zum einen längliche Aktin-Filamente, die in Zellen in der Regel Bestandteil des Zellskeletts sind.
Dazu gaben sie das Eiweiß Anilin, das in der Lage ist, die Aktin-Filamente miteinander zu verbinden und für Zellstabilität sorgt, und schließlich noch Myosin als molekularen Motor – denn um ihre Form verändern zu können, müssen die Zellen mit Hilfe solcher Motoren aktiv Kraft zu erzeugen.
Im Versuch beobachteten die Forscher, unter welchen Bedingungen sich die Modellzellen spontan verformen, die Zellskelett-Membran sich also entweder nach innen stülpt oder aber in bestimmten Bereichen eine Art Blase bildet, das so genannte Blebbing. Die Kräfte, die die äußere Form der Zelle verändern, wirken jeweils gegen die Lipidmembran.
„Das Zusammenspiel von Zellskelett und Membran ist der Schlüssel für alle Formveränderungen“, sagt Etienne Loiseau aus der Arbeitsgruppe Bausch und Erstautor der aktuellen Studie. „Bisher wurden Zytoskelett und Vesikel meist getrennt beobachtet, die Interaktionen dieser beiden essentiellen Komponenten konnte kaum untersucht werden.“
Konzentration auf das Wesentliche
Die in dem vom Exzellenzcluster Nanosystems Initiative Munich (NIM) geförderten Projekt aufgebaute Modellzelle kommt mit einer kleinen Anzahl von Komponenten aus. Auch die jeweiligen Konzentrationen der beteiligten Proteine lassen sich gezielt verändern und exakt kontrollieren.
Bausch und seine Kollegen zeigten, dass es auf die Wechselwirkung der Proteine in der Anwesenheit aller anderen Komponenten ankommt. Erst durch das Zusammenspiel der verschiedenen Komponenten entstehen biologische Funktionen. Offenbar ist auch die Konzentration der Komponenten entscheidend dafür, wie genau sich eine Zelle verformt.
„Erstaunlicherweise lässt sich mit denselben Proteinen einerseits eine Ausstülpung der Membran (blebbing) erreichen, während genau dasselbe System von Proteinen und Membran bei einer leicht anderen Konzentration einfach nur zu einer krassen Deformation führt“, sagt Bausch. „Es ist unerlässlich, die Interaktion der Proteine im Kontext zu verstehen – es sind die Wechselwirkungen der Proteine, die die Funktion ausmachen.“
Wirkmechanismen verstehen
Zwar gelingt es Biologen in aufwändigen zellbiologischen und biochemischen Experimenten die beteiligten Proteine oder Gene zu identifizieren, aufgrund der Komplexität der Zellen ist es aber meist nicht möglich, dabei auch die zugrundeliegenden Wirkmechanismen zu verstehen. „Unser „Bottom-up“-Ansatz auf Basis der synthetischen Zellmodelle hilft, wichtige Funktionsbeziehungen zu erkennen und zu erklären“, sagt Professor Bausch.
Noch funktionieren die Versuche zur Verformung von Zellen nur in statischen Systemen. Im nächsten Schritt wollen die Wissenschaftler versuchen, auch die dynamischen Prozesse nachzubauen, Bläschen im Zellmembran-Skelett also wie in der Natur entstehen und wieder verschwinden lassen und somit eine künstliche Modellzelle schaffen, die autonom existieren und sich auch fortbewegen kann.
Finanziell unterstützt wurden die Forschungsarbeiten mit Mitteln des European Research Council (ERC), der Deutschen Forschungsgemeinschaft (SFB 863 und Exzellenzcluster Nanosystems Initiative Munich). Proteininteraktionen wie diese stehen auch im Zentrum des Forschungsneubaus TUM Center for Protein Assemblies (CPA) der, aufgrund seiner überregionalen Bedeutung je zur Hälfte von Bund und Land gefördert, in den nächsten zwei Jahren auf dem Campus Garching entstehen soll.
[alert-warning]Publikation
Etienne Loiseau, Jochen A. M. Schneider, Felix C. Keber, Carina Pelzl, Gladys Massiera, Guillaume Salbreux, Andreas R. Bausch.
Shape remodeling and blebbing of active cytoskeletal vesicles.
Science Advances, Vol. 2, no. 4, e1500465, Apr. 15, 2016.
DOI: 10.1126/sciadv.1500465
Kontakt
Prof. Dr. Andreas Bausch
Technische Universität München
Lehrstuhl für Zellbiophysik (E27)
[/alert-warning]