1,4-Butandiol, auch als Butan-1,4-diol oder BDO bezeichnet, ist eine chemische Verbindung aus der Gruppe der gesättigten Diole. Die farb- und geruchlose, schwer entzündbare aber brennbare Flüssigkeit ist ein Intermediat der chemischen Industrie, welches vielfältige Anwendung findet.
BDO Herstellung
In der großtechnischen Synthese von 1,4-Butandiol in der chemischen Industrie werden verschiedene Verfahren eingesetzt. Das zweistufige Reppe-Verfahren (Ethinylierung) ist das älteste und am häufigsten verwendete. Dieses Verfahren, entwickelt von BASF-Chemiker Walter Reppe in den 1930er Jahren, basiert auf der Umsetzung von Acetylen mit 10–30%iger Formaldehyd-Lösung unter Verwendung von Bismut-modifizierten Kupfer(I)-acetylid-Katalysatoren auf Siliciumdioxid-Trägern. Die Reaktion erfolgt bei Temperaturen von 65–90 °C und Drücken von 0,9–10 bar, um 2-Butin-1,4-diol zu erzeugen. Dabei entsteht auch Propargylalkohol als Nebenprodukt, das abgetrennt und erneut in den Prozess zurückgeführt wird. Die Selektivität für 2-Butin-1,4-diol beträgt >90 % in Bezug auf Formaldehyd und etwa 80 % in Bezug auf Acetylen. Die Reaktion verläuft in einer Kaskade von Festbettreaktoren, die im Sumpf- oder Rieselfahrweise betrieben werden.
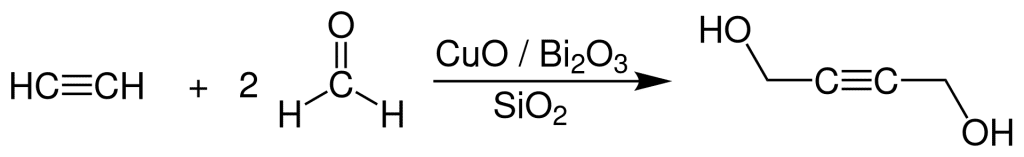
Im zweiten Schritt wird das erzeugte 2-Butin-1,4-diol in mehreren Stufen zu 1,4-Butandiol hydriert. Diese Hydrierung findet bei Temperaturen von 70–220 °C und Drücken von 150–300 bar (Festbett- oder Rieselphasenhydrierung) oder 10–65 bar (Suspension– oder Flüssigphasenhydrierung) statt. Sie verwendet Raney-Nickel-Katalysatoren mit zusätzlichen Promotoren wie Kupfer oder Chrom. Die Selektivität für 1,4-Butandiol beträgt 95 % in Bezug auf 2-Butin-1,4-diol. Die Hydrierung erfolgt in verschiedenen Reaktoren wie Strahldüsen-, Rührkessel- oder Blasensäulenreaktoren. Die Reinigung und Aufbereitung des Endprodukts erfolgen durch mehrstufige Destillation in Rektifikationskolonnen.
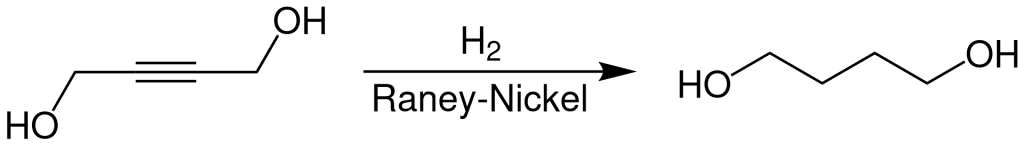
Bei dem Linde/Yukong-Prozess, der Weiterentwicklung des Reppe-Verfahrens, arbeitet man mit vergleichsweise niedrigen Drücken von ca. 1,4 bar.
Alternative Verfahren
Bei einem neueren Verfahren zur Herstellung von BDO oxidiert Propen zuerst zu Propylenoxid. Dann erfolgt die Isomerisierung zu Allylalkohol, gefolgt von der Hydroformylierung zu 4-Hydroxybutyraldehyd. Dieser Aldehyd wird schließlich zu 1,4-Butandiol hydriert.
Eine weitere alternative Methode zur Herstellung von 1,4-Butandiol ist der Davy-Prozess. Hierbei dient Maleinsäureanhydrid als Ausgangsmaterial.
BDO Produzenten
Die BASF SE ist der weltweit größte Hersteller von 1,4-Butandiol mit einer Gesamtkapazität von 670.000 Jahrestonnen. Sie betreibt Produktionsanlagen in verschiedenen Ländern, darunter Deutschland, die USA, Malaysia, China und Japan. Die Produktion erfolgt nicht nur nach dem Reppe-Verfahren, sondern auch mithilfe biotechnologischer Fermentation unter Verwendung von Hochleistungsmikroorganismen und nachwachsenden Rohstoffen. Weitere bedeutende Hersteller in diesem Bereich sind LyondellBasell und INEOS Solvents.
1,4-Butandiol Eigenschaften
1,4-Butandiol hat eine relative Gasdichte von 3,11 und eine relative Dichte des Dampf-Luft-Gemisches von 1,00 bei 20 °C und Normaldruck. Der Dampfdruck bei 20 °C beträgt weniger als 1 hPa, und die dynamische Viskosität liegt bei 71,5 mPa·s bei 25 °C.
BDO ist ein nicht leicht entzündbares, brennbares Terminaldiol und gehört zur Gruppe der Alkohole. Es ist eine schwer flüchtige Substanz, vollständig mit Wasser mischbar und gut in Ethanol und Dimethylsulfoxid löslich. Gefährliche chemische Reaktionen können auftreten, wenn es mit starken Oxidationsmitteln, Reduktionsmitteln, Säurechloriden und Säureanhydriden in Kontakt kommt. Eine wässrige 1,4-Butandiol-Lösung mit einer Konzentration von 500 g·l−1 hat bei 20 °C einen pH-Wert von 7–8.
Verwendung
1,4-Butandiol ist ein bedeutsames Zwischenprodukt in der chemischen Industrie, das als Ausgangsstoff für verschiedene Produkte wie Polyester, Polyamide und Polyurethane dient. Es wird auch zur Herstellung von Tetrahydrofuran verwendet, einem wichtigen Lösungsmittel und Ausgangsstoff für den Kunststoff PolyTHF®. Des Weiteren wird es bei der Synthese von Lösungsmitteln wie N-Methyl-2-pyrrolidon und γ-Butyrolacton eingesetzt. Darüber hinaus reagiert es mit Phosgen zur Bildung von Polycarbonaten und dient als Baustein für Polyester- und Polyetherpolyole. Im medizinischen Bereich dient BDO zur Herstellung von Busulfan.
Sicherheitshinweise
1,4-Butandiol wird hauptsächlich über den Atemtrakt und die Haut aufgenommen und verursacht nur geringfügige Reizungen der Schleimhäute. Es kann jedoch das Zentralnervensystem beeinträchtigen. Es wurden keine Hinweise auf Reproduktionstoxizität, Mutagenität oder Kanzerogenität in Tests und Tierversuchen gefunden. Die untere Explosionsgrenze beträgt 1,8 Vol.-% (67 g/m3), die obere Explosionsgrenze 15,7 Vol.-% (585 g/m3). Die Zündtemperatur liegt bei etwa 370 °C, was es in die Temperaturklasse T2 einordnet. Aufgrund eines Flammpunkts von etwa 130 °C gilt BDO als schwer entflammbar.
Dieser Eintrag basiert auf dem Artikel 1,4-Butandiol aus der freien Enzyklopädie Wikipedia. Es gilt die GNU-Lizenz für freie Dokumentation. Eine Liste der Autoren ist auf Wikipedia verfügbar.